
เนื้อหา
- ฟังก์ชัน
- โครงสร้าง
- ความสำคัญของตัวเร่งปฏิกิริยา
- ปัจจัยที่มีผลต่อประสิทธิผลของตัวเร่งปฏิกิริยา
- การใช้ catalase อื่น ๆ
คาตาเลสเป็นเอนไซม์ที่พบในเซลล์ของสัตว์พืชและแบคทีเรียแอโรบิก เอนไซม์เป็นโมเลกุลขนาดใหญ่สังเคราะห์ในเซลล์และผลิตเพื่อทำหน้าที่เป็นตัวเร่งปฏิกิริยาในปฏิกิริยา เอนไซม์แต่ละชนิดทำหน้าที่เฉพาะและหน้าที่ของ catalase คือการแปลงผลพลอยได้ที่อาจเป็นอันตรายให้เป็นองค์ประกอบที่มีประโยชน์สำหรับเซลล์

ฟังก์ชัน
Catalase เหมือนกับเอนไซม์ส่วนใหญ่เป็นโปรตีน มันถูกพบใน peroxisomes ซึ่งเป็น organelles เซลล์เยื่อ คาตาเลสมีหน้าที่ทางชีวภาพที่สำคัญ: เร่งปฏิกิริยาการสลายของไฮโดรเจนเปอร์ออกไซด์ซึ่งเป็นสารที่เป็นพิษต่อสิ่งมีชีวิตลงไปในน้ำและออกซิเจนโมเลกุลซึ่งทั้งไม่เป็นอันตรายและมีประโยชน์

โครงสร้าง
โครงสร้างดัมเบลของคาตาเลสประกอบด้วยโซ่โพลีเปปไทด์สี่สายแต่ละอันมีกรดอะมิโนมากกว่า 500 ตัว Catalase ยังมีกลุ่ม heme สี่กลุ่มซึ่งทำจากวงแหวนโพรพอฟฟีรินซึ่งมีอะตอมเหล็กเดียว แหวนเหล่านี้ตั้งอยู่ภายในสี่โซ่
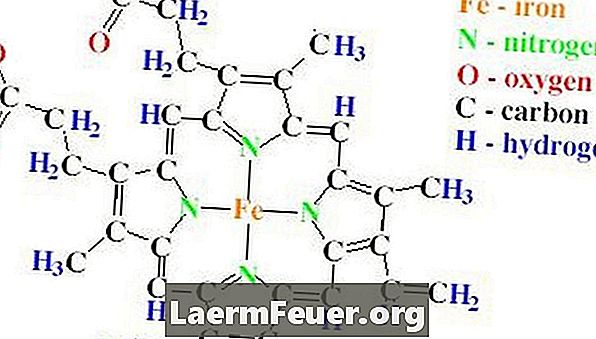
ความสำคัญของตัวเร่งปฏิกิริยา
ไฮโดรเจนเปอร์ออกไซด์เป็นผลพลอยได้จากการทำงานของสิ่งมีชีวิตมากมาย สิ่งมีชีวิตแบบแอโรบิคทั้งหมดใช้ออกซิเจนในการหายใจ การลดลงของออกซิเจนในน้ำมักจะไม่สมบูรณ์และอิเล็กตรอนพิเศษจากโลหะไอออนสามารถถ่ายโอนทำให้เกิดการก่อตัวของเปอร์ออกไซด์ อย่างไรก็ตามไฮโดรเจนเปอร์ออกไซด์ส่วนใหญ่ถูกสร้างขึ้นในระหว่างการผลิต ATP ในไมโตคอนเดรีย แม้ว่าไฮโดรเจนเปอร์ออกไซด์จะเป็นพิษต่อเซลล์ที่มีชีวิต แต่ปฏิกิริยาในการแตกกลับสู่น้ำและออกซิเจนก็เกิดขึ้นอย่างรวดเร็วและมีประสิทธิภาพ คาตาเลสเป็นที่รู้จักในฐานะหนึ่งในเอนไซม์ที่มีประสิทธิภาพที่สุดโดยมีการหมุนเวียนประมาณ 200,000 เหตุการณ์ / วินาที / หน่วยย่อย หากไม่มีตัวเร่งปฏิกิริยาเพื่อเพิ่มอัตราการเกิดปฏิกิริยาไฮโดรเจนเปอร์ออกไซด์จะยังคงอยู่ทำให้เซลล์เสียหาย
ปัจจัยที่มีผลต่อประสิทธิผลของตัวเร่งปฏิกิริยา
Catalase และอัตรากิจกรรมของมันจะถูกเปลี่ยนแปลงโดยปัจจัยหลายอย่างรวมถึงอุณหภูมิ, pH, ความเข้มข้นของเกลือ, ปริมาณของสารตั้งต้นและการปรากฏตัวของสารยับยั้งหรือ activators อุณหภูมิเป็นปัจจัยสำคัญในปฏิกิริยาทางชีวเคมีทั้งหมดเนื่องจากอุณหภูมิที่สูงอาจทำให้เกิดการสูญเสียสภาพของเอนไซม์ เมื่อเอนไซม์ถูกทำลายสภาพมันจะเปลี่ยนโครงสร้างทำให้สารตั้งต้นนั้นจับกันได้อย่างมีประสิทธิภาพน้อยลงซึ่งจะทำให้อัตราการเกิดปฏิกิริยาลดลง ในทางกลับกันจนกว่าจะถึงอุณหภูมิสูงสุด (ซึ่งแตกต่างกันสำหรับแต่ละประเภทของ catalase) ถึงอัตราการเกิดปฏิกิริยาจะเพิ่มขึ้นพร้อมกับอุณหภูมิ ค่า pH, การวัดความเป็นกรดหรือความเข้มข้นของไอออนไฮโดรเจนในสารละลายวัดได้ในระดับ 0 ถึง 14 เนื่องจากสารละลายมีความเป็นกรดมากขึ้น (ต่ำกว่า 7) เอนไซม์จะได้รับไฮโดรเจนไอออนจากสารละลาย และเมื่อวิธีการแก้ปัญหาพื้นฐานมากขึ้น (สูงกว่า 7) อาจสูญเสียไฮโดรเจนไอออน หนึ่งในสุดขั้วเหล่านี้สามารถลดอัตราการเกิดปฏิกิริยาเนื่องจากการเปลี่ยนแปลงพันธะเคมีของตัวเร่งปฏิกิริยา ตัวยับยั้งมีสองประเภท: noncompetitive inhibitors ซึ่งเชื่อมโยงกับไซต์ที่ไม่ได้เป็นไซต์ที่ใช้งานอยู่และตัวยับยั้งการแข่งขันซึ่งผูกกับไซต์ที่ใช้งานของ catalase คอปเปอร์ซัลเฟตเป็นตัวยับยั้งที่ไม่สามารถแข่งขันได้ของคาตาเลสและไซยาไนด์เป็นที่รู้จักกันว่าเป็นตัวยับยั้งการแข่งขัน โดยทั่วไปเมื่อปริมาณของไฮโดรเจนเปอร์ออกไซด์เพิ่มขึ้นอัตราการเกิดปฏิกิริยาก็จะเพิ่มขึ้นเช่นกัน อย่างไรก็ตามปฏิกิริยาของเอนไซม์เป็นไปตามสมการ Michaelis-Menten ซึ่งบอกว่าทุกปฏิกิริยาจะไปถึงจุดอิ่มตัวซึ่งหมายความว่าในอัตราการเกิดปฏิกิริยาสูงสุดการเติมสารตั้งต้นเพิ่มเติมจะไม่มีผลอีกต่อไป
การใช้ catalase อื่น ๆ
เนื่องจาก catalase มีอยู่ในสิ่งมีชีวิตแทบทุกชนิดมันเป็นหนึ่งในเอนไซม์ที่ศึกษามากที่สุด สิ่งนี้ทำให้นักวิทยาศาสตร์ค้นหาฟังก์ชันอื่นสำหรับเอนไซม์ที่มีประสิทธิภาพนี้ Catalase ใช้ในการรักษาด้านในของพลาสติกเพื่อบรรจุอาหาร มันป้องกันการเกิดออกซิเดชันและช่วยในการอนุรักษ์อาหาร คาตาเลสยังใช้ในกระบวนการฆ่าเชื้อแบบเย็นซึ่งเป็นกระบวนการในการเก็บรักษานมและชีสโดยการรักษาด้วยไฮโดรเจนเปอร์ออกไซด์ เอนไซม์นี้ใช้เพื่อลบร่องรอยของไฮโดรเจนเปอร์ออกไซด์ที่เหลืออยู่